C’est précisément là qu’intervient l’intelligence artificielle du jour. Oubliez les microscopes traditionnels et les expériences en laboratoire longues de plusieurs mois. Aujourd’hui, nous plongeons dans le code de la vie avec AlphaGenome, le dernier prodige de Google DeepMind. Cette IA n’est pas juste un outil de plus ; c’est un traducteur universel pour le langage complexe de notre génome.
Dans cet article, nous allons découvrir ensemble qui est AlphaGenome, remonter le fil de son histoire fascinante, et surtout, nous allons soulever le capot pour comprendre, avec des mots simples, comment il parvient à déchiffrer ces instructions cachées. Accrochez-vous, nous partons explorer la matière noire de notre biologie.
La carte d’identité de l’IA
- Nom : AlphaGenome
- Créateur : Google DeepMind
- Date de lancement : Prépublication en juin 2025, ouverture de l’API pour la recherche en juillet 2025
- Type d’IA : Modèle de Deep Learning multimodal spécialisé dans la prédiction de la régulation génomique
- Modèle de tarification : Accès gratuit via une API pour la recherche non-commerciale. Le futur modèle commercial n’a pas encore été précisé
- Langues supportées : Non applicable, l’IA traite des données biologiques (séquences d’ADN)
Pour faire simple, AlphaGenome est un peu l’équivalent d’un expert en linguistique ancienne qui, au lieu de déchiffrer des hiéroglyphes, décode la manière dont nos gènes sont activés ou désactivés.

Il était une fois… L’histoire d’AlphaGenome
L’épopée d’AlphaGenome ne commence pas dans un laboratoire de biologie, mais dans l’esprit des chercheurs de DeepMind, une startup londonienne fondée en 2010 avec une mission presque prophétique : « résoudre l’intelligence ». Rachetée par Google en 2014, cette équipe a rapidement prouvé que ses IA pouvaient exceller bien au-delà des jeux vidéo.
La saga « Alpha » est devenue leur marque de fabrique. Tout a commencé en 2016 avec AlphaGo, l’IA qui a battu le champion du monde de Go, un exploit que beaucoup pensaient impossible pour une machine. Ce succès a démontré la puissance de leurs approches pour résoudre des problèmes combinatoires immenses. Le jeu de Go, avec ses possibilités quasi infinies, n’était finalement qu’un terrain d’entraînement.
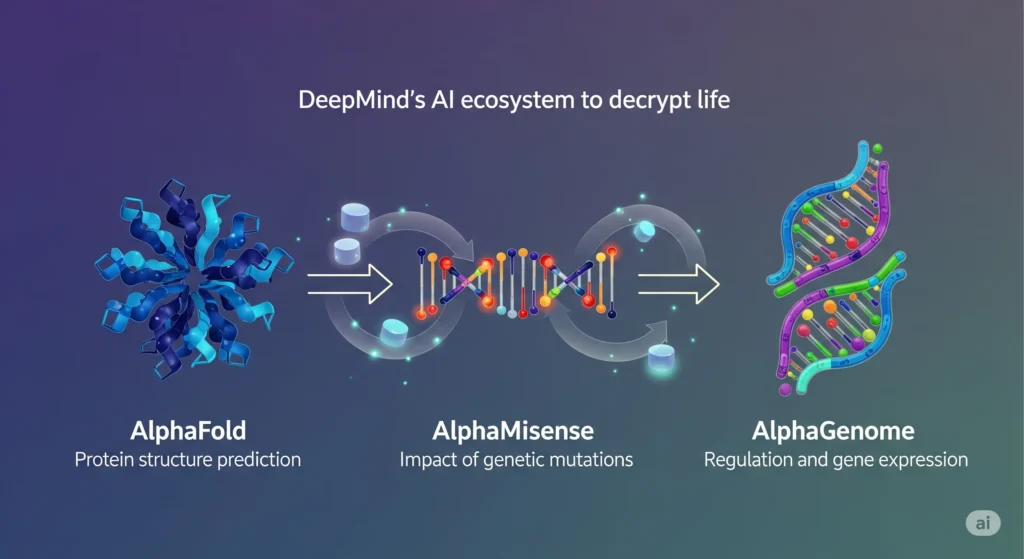
La véritable ambition de DeepMind était de s’attaquer à des défis scientifiques fondamentaux. C’est ainsi qu’en 2020, le monde a découvert AlphaFold, une révolution en biologie structurale. Cette IA a résolu le « problème du repliement des protéines », une énigme vieille de 50 ans, en prédisant la structure 3D de centaines de millions de protéines avec une précision stupéfiante. C’était comme obtenir le plan de montage de toutes les pièces d’un moteur complexe, ouvrant des portes incroyables pour la conception de médicaments.
Continuant sur sa lancée, DeepMind a dévoilé AlphaMissense en 2024, une IA capable de prédire l’impact des mutations génétiques « faux-sens »1, aidant à distinguer les mutations bénignes de celles pouvant causer des maladies.
Chaque « Alpha » s’appuyait sur les succès du précédent, s’attaquant à des problèmes de plus en plus complexes. Mais il restait un continent inexploré : la régulation des gènes. Savoir quelle protéine existe (AlphaFold) et comment une mutation peut l’altérer (AlphaMissense) est une chose. Comprendre pourquoi un gène est activé dans une cellule de foie et pas dans un neurone en est une autre.
Le développement d’AlphaGenome a été lancé pour relever ce défi. L’équipe a compris que pour prédire l’effet des mutations dans les 98% non codants du génome, il fallait un modèle capable de « lire » et de « comprendre » des séquences d’ADN extraordinairement longues. Les modèles existants peinaient au-delà de quelques milliers de « lettres » (paires de bases) d’ADN. Le défi technique était immense : analyser des segments contenant jusqu’à un million de paires de bases pour capturer les interactions à longue distance.
En juin 2025, le fruit de ce travail a été révélé dans une prépublication scientifique qui a fait l’effet d’une bombe. On y découvrait une architecture hybride, une chimère technologique combinant le meilleur de deux mondes de l’IA. Un mois plus tard, en juillet 2025, fidèle à sa mission de faire progresser la science, DeepMind a ouvert une API pour permettre aux chercheurs du monde entier d’utiliser AlphaGenome gratuitement pour des projets non-commerciaux. La chasse aux secrets de la « matière noire » du génome était officiellement ouverte.
Comment ça marche ?
Tenter de comprendre comment nos gènes sont régulés, c’est comme essayer de comprendre le trafic d’une mégalopole en ne regardant qu’une seule rue. AlphaGenome, lui, a une vue satellite en temps réel de toute la ville. Voyons comment.
Niveau 1 – Vue d’ensemble : Le GPS du génome
L’analogie centrale pour comprendre AlphaGenome est celle d’un système de navigation GPS ultra-perfectionné pour notre ADN.
Imaginez que vous donniez à ce GPS une très longue adresse, une séquence d’ADN brute pouvant atteindre un million de lettres (les fameuses paires de bases). Votre GPS ne se contente pas de vous dire « vous êtes ici ». En une fraction de seconde, il va scanner toute la zone et vous fournir une carte interactive complète.
Sur cette carte, il va :
- Identifier les « bâtiments » importants : les gènes eux-mêmes.
- Afficher les « routes d’accès » : les régions de l’ADN qui sont ouvertes et accessibles (l’accessibilité chromatinienne).
- Signaler les « feux de circulation » et les « interrupteurs » : les endroits précis où les protéines régulatrices se lient à l’ADN pour allumer ou éteindre les gènes.
- Prédire les « flux de trafic » : l’intensité à laquelle un gène sera lu et transcrit (l’expression génique).
- Anticiper les « déviations » et les « raccourcis » : il prédit comment la séquence d’un gène sera « découpée et recollée » avant d’être traduite en protéine (un processus crucial appelé épissage ou splicing).
En somme, quand vous donnez un morceau d’ADN à AlphaGenome, il ne se contente pas de le lire. Il vous raconte son histoire, sa fonction et son rôle dans l’immense ville qu’est la cellule.
Niveau 2 – Sous le capot : Les deux experts de l’IA
Pour réaliser cette prouesse, AlphaGenome s’appuie sur une architecture qui combine deux des plus grandes stars de l’IA moderne : les Réseaux de Neurones Convolutifs (CNN) et les Transformeurs.
- Le spécialiste local : le CNN, un détective de proximité.
- Qu’est-ce qu’un CNN ? C’est une IA spécialisée dans la reconnaissance de motifs dans des données, un peu comme un logiciel de reconnaissance faciale trouve un nez ou des yeux sur une photo.
- Son rôle dans AlphaGenome : Le CNN balaie la séquence d’ADN et agit comme un détective qui cherche des indices locaux. Il est entraîné à repérer des séquences courtes et spécifiques, des « mots-clés » de quelques lettres qui sont souvent des sites d’amarrage pour les protéines régulatrices. Pensez à lui comme à un expert qui lit les étiquettes sur chaque porte d’un immense couloir pour savoir ce qu’il y a derrière.
- Le stratège global : le Transformeur, un visionnaire à longue distance.
- Qu’est-ce qu’un Transformeur ? C’est le type d’architecture qui a fait le succès des IA comme ChatGPT. Sa superpuissance est de comprendre le contexte et les relations entre des éléments très éloignés les uns des autres. C’est ce qui permet à une IA de comprendre qu’un mot au début d’un paragraphe peut changer le sens d’un mot à la toute fin.
- Son rôle dans AlphaGenome : L’ADN n’est pas une simple ligne droite ; il se replie sur lui-même dans le noyau de la cellule. Deux morceaux d’ADN qui sont très éloignés sur la séquence linéaire peuvent en réalité être voisins dans l’espace 3D et interagir. Le Transformeur est celui qui modélise ces interactions à longue distance. Il comprend que l’interrupteur qui se trouve à 500 000 lettres de distance peut en fait contrôler le gène juste « à côté ». Il voit la carte entière, pas seulement la rue.
En combinant ces deux experts, AlphaGenome obtient le meilleur des deux mondes : une analyse fine des détails locaux (CNN) intégrée dans une compréhension globale du contexte génomique (Transformeur). C’est cette synergie qui lui permet de surpasser les modèles précédents.
Concurrence et positionnement
AlphaGenome n’est pas arrivé dans un vide. Le champ de la génomique computationnelle est en pleine effervescence. Ses principaux « rivaux » ou prédécesseurs incluent :
- Enformer : Également développé par DeepMind, il était le précédent champion de la prédiction à partir de longues séquences. AlphaGenome est en quelque sorte sa version améliorée, notamment plus précise sur le phénomène crucial de l’épissage.
- Basenji : Un modèle développé par des chercheurs universitaires, très efficace mais se concentrant principalement sur l’expression génique locale.
- SpliceAI : Comme son nom l’indique, c’est un outil ultra-spécialisé et très performant pour prédire l’épissage, mais sans la vision d’ensemble du contexte génomique à longue portée qu’offre AlphaGenome.
Ce qui différencie vraiment AlphaGenome, c’est sa capacité à faire tout en même temps et à grande échelle. Là où les autres étaient des spécialistes (le sprinteur, le sauteur en hauteur), AlphaGenome est le décathlonien de classe olympique. Il traite des séquences extrêmement longues, intègre la prédiction de l’épissage directement dans son modèle global, et le fait avec une efficacité redoutable (un entraînement complet ne prendrait que quelques heures sur le matériel adéquat).
Points forts et cas d’usage
La véritable valeur d’une IA se mesure à ce qu’elle permet de faire. Voici quelques exemples concrets du potentiel d’AlphaGenome.
Points forts clés :
- Vision holistique2 : Il offre la prédiction la plus complète à ce jour, liant des milliers de propriétés moléculaires à partir d’une seule séquence d’ADN.
- Performance supérieure : Dans les tests, il surpasse les modèles existants, y compris les plus spécialisés, sur la grande majorité des tâches de prédiction (24 des 26 benchmarks d’évaluation).
- Accessibilité : En ouvrant une API gratuite aux chercheurs, DeepMind accélère la recherche fondamentale à l’échelle mondiale.
Cas d’usage concrets :
1. Identifier la source génétique de cancers
- Problème : De nombreux cancers sont causés par des mutations dans l’ADN non codant, qui agissent comme des interrupteurs défectueux. Identifier la bonne mutation parmi des milliers est comme chercher une aiguille dans une botte de foin.
- Mini-tutoriel :
- Un chercheur isole une séquence d’ADN d’une tumeur, contenant plusieurs mutations candidates dans une région non codante.
- Il soumet cette séquence à l’API AlphaGenome pour obtenir une carte de base de la régulation dans cette zone.
- Ensuite, il soumet virtuellement la même séquence mais en introduisant une à une les mutations suspectes (in silico).
- AlphaGenome prédit l’impact de chaque mutation : l’une d’elles provoque-t-elle un changement radical dans l’épissage d’un gène suppresseur de tumeur ? Ou active-t-elle un gène favorisant la croissance cellulaire ?. C’est ainsi qu’AlphaGenome a pu simuler une mutation clé impliquée dans une forme de leucémie.
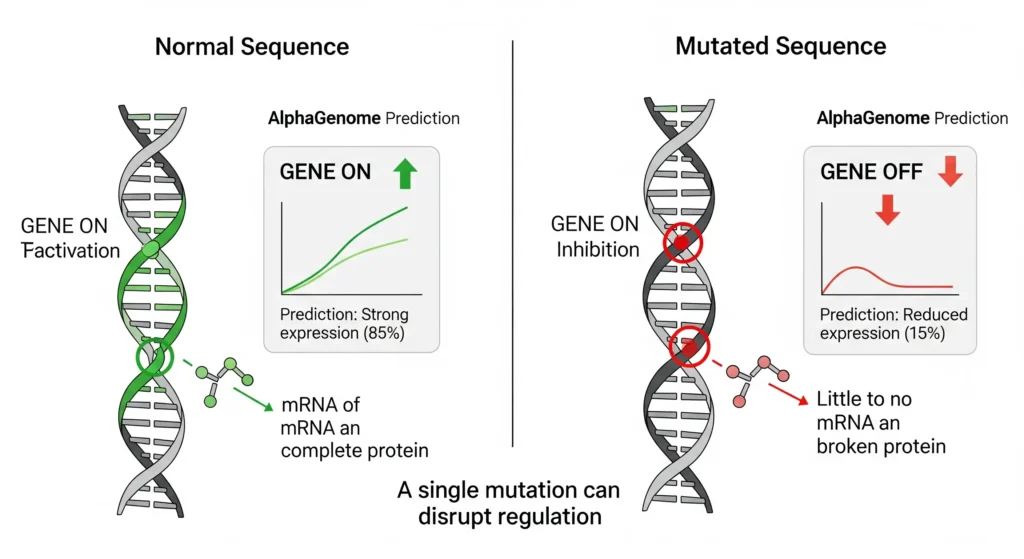
2. Résoudre des énigmes de maladies rares
- Problème : Un patient souffre d’une maladie génétique rare, mais l’analyse des gènes codants ne révèle aucune anomalie. La cause est probablement cachée dans les 98% restants.
- Mini-tutoriel :
- Le génome complet du patient est séquencé.
- Les régions non codantes sont analysées et comparées au génome de référence.
- Les variants génétiques uniques au patient sont soumis à AlphaGenome.
- L’IA prédit si l’un de ces variants perturbe un « locus régulateur » critique, c’est-à-dire un interrupteur majeur contrôlant un gène essentiel, même s’il est situé très loin sur le chromosome.
3. Concevoir des gènes sur mesure en biologie synthétique
- Problème : Des scientifiques veulent créer un gène synthétique qui ne s’exprime que dans un type de cellule très spécifique (ex: pour une thérapie génique).
- Mini-tutoriel :
- Les chercheurs conçoivent une séquence de gène « codante » pour la protéine qu’ils souhaitent produire.
- Ils utilisent AlphaGenome pour tester différentes séquences « non codantes » (promoteurs, enhancers) à y attacher.
- L’IA simule l’efficacité de chaque construction, prédisant laquelle sera la plus stable, la mieux exprimée et la plus spécifique au tissu cellulaire visé, optimisant ainsi le design avant même de synthétiser la moindre molécule d’ADN en laboratoire.
Limites, risques et points faibles
AlphaGenome est un outil surpuissant, mais il n’est pas magique.
- La distance a son importance : Bien qu’il analyse des séquences très longues, sa précision prédictive commence à diminuer lorsque les éléments en interaction sont séparés par plus de 100 000 paires de bases. La carte devient un peu plus floue sur les très longues distances.
- Le diable est dans les détails cellulaires : Le modèle est très performant pour prédire une « moyenne » de la régulation, mais il peine encore à capturer toutes les nuances subtiles spécifiques à chaque type de cellule (un neurone vs une cellule de peau) ou aux différentes étapes du développement embryonnaire.
- De la séquence au symptôme, il y a un monde : AlphaGenome prédit des mécanismes moléculaires (le gène X est moins exprimé), mais il ne peut pas prédire directement des traits complexes comme le risque de diabète ou la couleur des yeux. Il nous donne une pièce du puzzle, pas l’image complète de la boîte.
- Le risque de la boîte noire : Comme pour toute IA complexe, il peut être difficile de savoir pourquoi le modèle a fait une prédiction spécifique. L’interprétabilité (on en reparlera bientôt) reste un défi majeur pour une adoption en clinique, où les médecins ont besoin de comprendre le raisonnement derrière un diagnostic.
Il faut voir AlphaGenome comme un instrument de recherche phénoménal, qui génère des hypothèses incroyablement précises que les biologistes devront ensuite confirmer par des expériences ciblées.
Conclusion
AlphaGenome n’est pas simplement une nouvelle version d’un outil existant. C’est un changement de paradigme dans notre façon d’interroger le livre de la vie. En parvenant à lire et interpréter la grammaire complexe de notre ADN non codant, cette IA de Google DeepMind nous ouvre les portes des 98% de notre génome qui restaient largement une énigme. Elle transforme cette « matière noire » biologique en une carte lisible, pleine d’interrupteurs, de chemins et de signaux.
Plus qu’un simple prédicteur, c’est un simulateur. Un laboratoire virtuel où l’on peut tester l’effet d’une mutation en quelques secondes au lieu de plusieurs mois. Son véritable impact se mesurera à travers les découvertes qu’il va permettre dans la recherche sur le cancer, les maladies rares et la biologie fondamentale.
La question n’est plus de savoir si nous allons comprendre le langage de notre génome, mais à quelle vitesse. AlphaGenome vient de nous donner la Pierre de Rosette que nous attendions. Et maintenant, que lirons-nous en premier dans ce grand livre ouvert ?

Le sujet vous passionne ? Vous êtes chercheur ou simplement curieux ?
- La question du jour : Selon vous, quelle sera l’application la plus révolutionnaire d’AlphaGenome à long terme : la médecine personnalisée, la conception de nouvelles thérapies ou la réécriture de nos manuels de biologie ? Partagez votre avis dans les commentaires !
- Défi pour les connaisseurs : Si vous aviez accès à l’API, quelle énigme biologique ou quelle maladie génétique non résolue choisiriez-vous d’explorer en premier avec la puissance d’AlphaGenome ?
Pour approfondir le sujet :
- L’article de Nature (en anglais) : Pour une vue d’ensemble journalistique et scientifique : « DeepMind’s new AlphaGenome AI predicts the function of the genome’s ‘dark matter’ »
- L’annonce sur le blog de DeepMind (en anglais) : Pour la vision des créateurs (consultez les archives du blog DeepMind pour juillet 2025).
- L’article technique d’InfoQ (en anglais) : Pour ceux qui veulent plus de détails sur l’architecture : « Google DeepMind Unveils AlphaGenome to Predict Gene Regulation »
Timeline des dates clés
- 2010 : Fondation de la startup DeepMind à Londres.
- 2014 : Rachat de DeepMind par Google.
- 2016 : AlphaGo bat le champion du monde Lee Sedol, démontrant la puissance de l’IA de DeepMind.
- 2020 : AlphaFold résout le problème du repliement des protéines, une avancée majeure en biologie.
- Juin 2025 : Publication de la prépublication scientifique décrivant l’architecture et les performances d’AlphaGenome.
- Juillet 2025 : Ouverture de l’API de recherche non-commerciale d’AlphaGenome à la communauté scientifique.
Glossaire des termes médicaux de cet article :
- ADN non codant : Les 98% de notre génome qui ne contiennent pas les instructions directes pour fabriquer des protéines, mais qui jouent un rôle crucial dans la régulation de l’activité des gènes.
- Chromatine : Le complexe d’ADN et de protéines qui constitue nos chromosomes. Son « accessibilité » détermine si les gènes peuvent être lus ou non.
- Épissage (Splicing) : Un processus cellulaire qui, après la lecture d’un gène, « découpe » des parties non pertinentes (introns) et « recolle » les parties utiles (exons) pour former l’ARN messager final qui servira de recette pour une protéine. Des erreurs d’épissage peuvent causer de nombreuses maladies.
- Paire de bases : Les « lettres » de l’alphabet de l’ADN (A-T et C-G). Le génome humain en contient environ 3 milliards.
- Régulation génomique : L’ensemble des mécanismes complexes qui contrôlent quels gènes sont activés (« ON ») ou désactivés (« OFF ») dans une cellule, à un moment donné.
Dans le prochain article, nous allons revenir vers une IA européenne, qui ose se dresser face aux montres américains et chinois, une IA qui allemande qui utilise aussi le mot Alpha dans son patronyme, je veux parler d’Aleph Alpha. Abonnez-vous pour rien rater de mon actualité. Je vous donne rendez-vous dès demain pour ce nouvel article de la série 1 jour 1 IA !
Notes de bas de page
- Une mutation faux-sens est un changement d’une seule lettre dans l’ADN qui fait que la cellule fabrique une protéine différente avec un acide aminé modifié à une position précise. Cette modification peut rendre la protéine non fonctionnelle ou altérer son bon fonctionnement, ce qui peut provoquer des maladies génétiques comme la drépanocytose. ↩︎
- Une vision holistique consiste à appréhender une réalité comme un tout indivisible, plutôt que de la réduire à la somme de ses parties. L’adjectif holistique vient du grec « holos » signifiant « entier » ou « total ». Cette approche considère que chaque élément ou chaque problème ne peut être compris qu’en tenant compte de l’ensemble auquel il appartient. ↩︎
Vous pouvez retrouver tous les termes techniques de cet article dans le glossaire disponible ici.
⚠️ Avertissement sur la mise à jour des informations
Cet article a été rédigé en juin 2025. Le domaine de l’intelligence artificielle évoluant extrêmement rapidement, certaines informations présentées peuvent ne plus être à jour au moment de votre lecture. Je vous invite à vérifier les dernières actualités et développements dans ce secteur.
🤖 Méthodologie de rédaction & rôle de l’IA
J’ai rédigé cet article avec l’assistance de plusieurs outils d’intelligence artificielle : Perplexity pour les recherches documentaires, Gemini pour la rédaction des sections techniques et leur vulgarisation, et ChatGPT pour la génération des images.
Cet article s’inscrit dans la série « 1 jour – 1 IA », une démarche qui poursuit un double objectif : rendre accessible l’univers des intelligences artificielles par des contenus pédagogiques de qualité, tout en démontrant qu’il est possible de maintenir un rythme de publication quotidien sans sacrifier sa vie professionnelle et familiale, grâce aux bons outils.
Cette approche collaborative entre humain et IA illustre parfaitement les nouvelles méthodes de création de contenu : Perplexity a alimenté mes recherches documentaires avec ses réponses sourcées, Gemini m’a accompagné dans la vulgarisation des concepts techniques les plus complexes, tandis que ChatGPT a donné vie aux illustrations visuelles. Mon rôle d’auteur s’est concentré sur la conception initiale, l’architecture narrative, la cohérence stylistique et les ajustements pour préserver ma voix éditoriale. Cette synergie représente environ 50% de travail humain et 50% d’assistance IA.